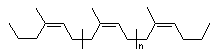|
1. Experiment ist im WACKER-Schulversuchskoffer enthalten |
nein |
2. Versuchsvorschrift wurde modifiziert |
/ |
3. Eigene Versuchsvorschrift wurde entwickelt |
ja |
4. Video-Clip verfügbar |
nein |
5. Flash-Animation verfügbar |
nein |
6. Weitere Materialien: Arbeitsblätter
4. |
|
 |
Chemikalienbeständigkeit von Silicongummi im
Vergleich zu anderen Elastomeren |
 |
  1
Materialien, Chemikalien, Zeitbedarf 1
Materialien, Chemikalien, Zeitbedarf |
 |
- Schnappdeckelgläser
- Federwaage + Quetsche
- Pinzette
- Waage
- verschiedene Gummiproben (Schuhsohle, Gummischlauch, Naturlatex)
- verschiedene Silicongummiproben aus dem WACKER-Schulversuchskoffer,
z.B. HTV sowie ein selbst hergestelltes
Siliconelastomer RTV2(r)
- Aceton, F
- Benzin (normal, unverbleit), F
- Salzsäure, c = 2 mol/l, konz. Salzsäure, C
- Natronlauge, c = 2 mol/l, konz. Natronlauge, w = 50
%, C
- Mineralöl (z.B. SAE 15 W 40), F
- Schwefelsäure, c = 1 mol/l, C
Eine genaue Zeitkalkulation anzugeben ist bei diesem
Versuch nicht möglich, da die Versuchszeit für die Probenvorbereitung,
Untersuchung etc., von der Anzahl der Schüler, Proben und Chemikalien
abhängt. |
 |
  2
Versuchsdurchführung und -beobachtung 2
Versuchsdurchführung und -beobachtung |
 |
| Beim Arbeiten mit den Chemikalien sind Schutzhandschuhe und Schutzbrille
zu tragen. |
 |
|
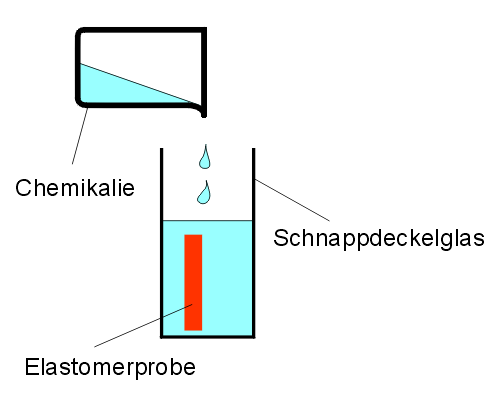
| Versuchsskizze:
Chemikalienbeständigkeit von Siliconen |
|
 |
  Zuerst
werden die verschiedenen Gummiproben in Form eines Rechtecks zurecht geschnitten.
Die Reißfestigkeit der Proben wird qualitativ mit der Hand und bei
einer Zugkraft von 10 N untersucht. Von jeder Probe wird die Masse bestimmt. Zuerst
werden die verschiedenen Gummiproben in Form eines Rechtecks zurecht geschnitten.
Die Reißfestigkeit der Proben wird qualitativ mit der Hand und bei
einer Zugkraft von 10 N untersucht. Von jeder Probe wird die Masse bestimmt.
Dann übergießt man im Schnappdeckelgläschen (alternativ
Reagenzglas) die Elastomerproben mit wenigen Millilitern der jeweiligen
Chemikalie und lässt die verschlossenen Schnappdeckelgläser
etwa eine Woche lang stehen.
Danach wird die Probe aus der Chemikalie herausgenommen, getrocknet und
die Masse erneut bestimmt. Man untersucht die Probe auf äußere
Veränderungen und auf Reißfestigkeit.
Die Versuchsbeobachtungen werden in einer Tabelle zusammengetragen und
die Chemikalienbeständigeit wird mit einer Zahl von 1-3 bewertet.
Dabei bedeutet 1 = sehr gut beständig (keine Veränderungen),
2 = durchschnittlich beständig (geringe Veränderungen, z.b.
Farbänderungen der Lösung) und 3 = wenig beständig (Stoff
wird stark angegriffen bzw. zerstört).
Nach Ablauf einer Woche wurden in einem Referenzversuch folgende Beobachtungen
gemacht:
  Elastomere
+ Aceton: Elastomere
+ Aceton:
|
 |
 |
 |
 |
 |
|
Masse in g |
Reißfestigkeit bei 10 N |
|
|
| Probe |
vorher |
nachher |
vorher |
nachher |
Beobachtung |
Chemikalien-
beständigkeit |
| Naturgummi |
/ |
/ |
ja |
ja |
Leicht aufgequollen,
sonst keine sichtbaren Veränderungen
Elastizität und Reißfestigkeit unverändert |
2 |
| Schuhsohle |
0,2 |
0,25 |
ja |
ja |
Die Flüssigkeit
färbt sich leicht gelb.
An der Sohle keine sichtbaren Veränderungen
Elastizität und Reißfestigkeit unverändert |
2 |
Gummi-
schlauch |
0,45 |
0,5 |
ja |
ja |
Die Flüssigkeit
färbt sich gelb.
Am Schlauch keine sichtbaren Veränderungen
Elastizität und Reißfestigkeit unverändert |
2 |
| HTV(b) |
0,3 |
0,3 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(s) |
0,3 |
0,35 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(w) |
0,55 |
0,37 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| RTV2(r) |
0,55 |
0,65 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
|
 |
| (Aufgrund der zu geringen Masse der Naturgummiproben wurde
diese nicht bestimmt.) |
 |
   |
 Foto
1: Elastomerproben nach einwöchiger Einwirkung von Aceton Foto
1: Elastomerproben nach einwöchiger Einwirkung von Aceton |
 |
  Elastomere
+ Benzin: Elastomere
+ Benzin: |
 |
 |
 |
 |
 |
|
Masse in g |
Reißfestigkeit bei 10 N |
|
|
| Probe |
vorher |
nachher |
vorher |
nachher |
Beobachtung |
Chemikalien-
beständigkeit |
| Naturgummi |
/ |
/ |
ja |
nein |
Keine äußerlichen
Veränderungen
Elastizität und Reißfestigkeit haben stark abgenommen. |
3 |
| Schuhsohle |
0,2 |
0,3 |
ja |
nein |
Die Probe
ist leicht aufgequollen.
Elastizität und Reißfestigkeit haben stark abgenommen. |
3 |
Gummi-
schlauch |
0,5 |
1,05 |
ja |
nein |
Die Probe
ist stark aufgequollen.
Elastizität und Reißfestigkeit haben stark abgenommen. |
3 |
| HTV(b) |
0,4 |
0,7 |
ja |
ja |
Die Probe
ist mittelstark aufgequollen.
Elastizität und Reißfestigkeit sind unverändert. |
2 |
| HTV(s) |
0,5 |
0,85 |
ja |
ja |
Die Probe
ist mittelstark aufgequollen.
Elastizität und Reißfestigkeit sind unverändert. |
2 |
| HTV(w) |
0,2 |
2 |
ja |
nein |
Probe ist
sehr stark aufgequollen.
Elastizität und Reißfestigkeit haben stark abgenommen. |
3 |
| RTV2(r) |
0,2 |
0,77 |
ja |
nein |
Probe ist
stark aufgequollen.
Elastizität und Reißfestigkeit haben stark abgenommen. |
3 |
|
 |
   |
 Foto
2: Elastomerproben nach einwöchiger Einwirkung von Benzin Foto
2: Elastomerproben nach einwöchiger Einwirkung von Benzin |
 |
  Elastomere
+ Salzsäure, c = 2 mol/l: Elastomere
+ Salzsäure, c = 2 mol/l: |
 |
 |
 |
 |
 |
|
Masse in g |
Reißfestigkeit bei 10 N |
|
|
| Probe |
vorher |
nachher |
vorher |
nachher |
Beobachtung |
Chemikalien-
beständigkeit |
| Naturgummi |
/ |
/ |
ja |
ja |
Die Probe
färbt sich leicht gelblich.
Elastizität und Reißfestigkeit unverändert |
2 |
| Schuhsohle |
0,3 |
0,3 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
Gummi-
schlauch |
0,35 |
0,4 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(b) |
0,45 |
0,5 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(s) |
0,3 |
0,3 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(w) |
0,3 |
0,3 |
ja |
ja |
Keine sichtbaren
Veränderunget
Elastizität und Reißfestigkeit unverändert |
1 |
| RTV2(r) |
0,4 |
0,4 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
|
 |
  Elastomere
+ Salzsäure, c = 10 mol/l (konz. Salzsäure): Elastomere
+ Salzsäure, c = 10 mol/l (konz. Salzsäure): |
 |
 |
 |
 |
 |
|
Masse in g |
Reißfestigkeit bei 10 N |
|
|
| Probe |
vorher |
nachher |
vorher |
nachher |
Beobachtung |
Chemikalien-
beständigkeit |
| Naturgummi |
/ |
/ |
ja |
ja |
Die Probe
färbt sich weiß.
Elastizität und Reißfestigkeit unverändert |
2 |
| Schuhsohle |
0,25 |
0,27 |
ja |
ja |
Die Lösung
färbt sich intensiv gelb.
Die Probe fühlt sich etwas härter an.
Elastizität und Reißfestigkeit unverändert |
2 |
Gummi-
schlauch |
0,25 |
0,3 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(b) |
0,45 |
Nicht messbar |
ja |
nein |
Die Lösung
färbt sich gelblich.
Die Probe selbst färbt sich intensiv dunkelblau und zerbröselt beim
Herausnehmen und in den Händen.
Nicht mehr elastisch und reißfest |
3 |
| HTV(s) |
0,3 |
0,25 |
ja |
ja |
Keine äußerlichen
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(w) |
0,3 |
0,3 |
ja |
ja |
Die Probe
wird etwas klebrig, sonst sind keine äußerlichen Veränderungen feststellbar.
Die Probe reißt etwas schneller, besteht aber den Test. |
2 |
| RTV2(r) |
0,6 |
0,7 |
ja |
nein |
Die Probe
färbt sich gelb und wird stark klebrig und schmierig.
Ebenso färbt sich die Lösung gelblich.
Die Probe ist nicht mehr elastisch und zerbricht beim Ziehen. |
3 |
|
 |
   |
 Foto
3: Elastomerproben nach einwöchiger Einwirkung von konz. Salzsäure Foto
3: Elastomerproben nach einwöchiger Einwirkung von konz. Salzsäure |
 |
  Elastomere
+ Natronlauge, c = 2 mol/l: Elastomere
+ Natronlauge, c = 2 mol/l: |
 |
 |
 |
 |
 |
|
Masse in g |
Reißfestigkeit bei 10 N |
|
|
| Probe |
vorher |
nachher |
vorher |
nachher |
Beobachtung |
Chemikalien-
beständigkeit |
| Naturgummi |
/ |
/ |
ja |
ja |
Die Probe
ist nicht mehr so transparent, sonst sind keine Veränderungen feststellbar.
Elastizität und Reißfestigkeit unverändert. |
1 |
| Schuhsohle |
0,2 |
0,2 |
ja |
ja |
Die Probe
ist etwas weicher geworden und die Lösung hat sich gelb gefärbt.
Die Elastizität hat etwas zugenommen. die Reißfestigkeit ist unverändert
geblieben. |
2 |
Gummi-
schlauch |
0,35 |
0,48 |
ja |
ja |
Die Probe
fühlt sich etwas weicher an.
Die Flüssigkeit hat sich intensiv gelb-orange gefärbt.
Elastisch, aber nicht mehr so reißfest |
2 |
| HTV(b) |
0,35 |
0,35 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(s) |
0,25 |
0,25 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(w) |
0,3 |
0,3 |
ja |
ja |
Die Probe
ist etwas klebrig, sonst sind keine äußerlichen Veränderungen erkennbar.
Elastizität und Reißfestigkeit unverändert |
1 |
| RTV2(r) |
0,27 |
0,28 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
|
 |
  Elastomere
+ Natronlauge, w = 50 %: Elastomere
+ Natronlauge, w = 50 %: |
 |
 |
 |
 |
 |
|
Masse in g |
Reißfestigkeit bei 10 N |
|
|
| Probe |
vorher |
nachher |
vorher |
nachher |
Beobachtung |
Chemikalien-
beständigkeit |
| Naturgummi |
/ |
/ |
ja |
ja |
Die Probe
ist nicht mehr so transparent, sonst sind keine Veränderungen feststellbar.
Elastizität und Reißfestigkeit unverändert |
1 |
| Schuhsohle |
0,2 |
0,25 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
Gummi-
schlauch |
0,922 |
0,908 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(b) |
0,223 |
0,192 |
ja |
ja |
Oberfläche
der Probe dunkelblau, bröselig und seifig
Unter der Oberfläche unverändert
Elastisch und reißfest |
3 |
| HTV(s) |
0,682 |
0,695 |
ja |
zu seifig zum Messen |
Die Oberfläche
der Probe ist klebrig und seifig.
Darunter ist die Probe unverändert.
Elastisch und reißfest |
3 |
| HTV(w) |
0,677 |
0,697 |
ja |
zu seifig zum Messen |
Die Oberfläche
der Probe ist klebrig und seifig.
Darunter ist die Probe unverändert.
Elastisch und reißfest |
3 |
| RTV2(r) |
0,645 |
0,639 |
ja |
ja |
Etwas seifig,
sonst keine Veränderungen
Elastizität und Reißfestigkeit unverändert |
2 |
|
 |
  Elastomere
+ Mineralöl SAE 15 W 40: Elastomere
+ Mineralöl SAE 15 W 40: |
 |
 |
 |
 |
 |
|
Masse in g |
Reißfestigkeit bei 10 N |
|
|
| Probe |
vorher |
nachher |
vorher |
nachher |
Beobachtung |
Chemikalien-
beständigkeit |
| Naturgummi |
/ |
/ |
ja |
nein |
Die Probe
ist leicht aufgequollen, sonst ist keine Veränderung feststellbar.
Fast nicht mehr elastisch
Reißtfestigkeit stark abgenommen |
3 |
| Schuhsohle |
0,25 |
0,28 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
Gummi-
schlauch |
0,3 |
0,43 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(b) |
0,3 |
0,303 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(s) |
0,27 |
0,276 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(w) |
0,25 |
0,246 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| RTV2(r) |
0,6 |
0,613 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
|
 |
   |
 Foto
4: Elastomerproben nach einwöchiger Einwirkung von Mineralöl SAE
15 W 40 Foto
4: Elastomerproben nach einwöchiger Einwirkung von Mineralöl SAE
15 W 40 |
 |
  Elastomere
+ Schwefelsäure, c = 1 mol/l: Elastomere
+ Schwefelsäure, c = 1 mol/l: |
 |
 |
 |
 |
 |
|
Masse in g |
Reißfestigkeit bei 10 N |
|
|
| Probe |
vorher |
nachher |
vorher |
nachher |
Beobachtung |
Chemikalien-
beständigkeit |
| Naturgummi |
/ |
/ |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| Schuhsohle |
0,2 |
0,246 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
Gummi-
schlauch |
0,2 |
0,249 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(b) |
0,5 |
0,42 |
ja |
ja |
Die Probe
hat sich etwas dunkler gefärbt, sonst ist keine Veränderung feststellbar.
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(s) |
0,2 |
0,235 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| HTV(w) |
0,25 |
0,255 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
| RTV2(r) |
0,6 |
0,637 |
ja |
ja |
Keine sichtbaren
Veränderungen
Elastizität und Reißfestigkeit unverändert |
1 |
|
 |
  3
Versuchsauswertung 3
Versuchsauswertung
|
 |
| Anhand der Beobachtungen kann für die Chemikalienbeständigkeit
der untersuchten Elastomere bei Raumtemperatur folgende Tabelle aufgestellt
werden: |
 |
| |
Naturgummi |
Schuhsohle |
Gummischlauch |
HTV(b) |
HTV(s) |
HTV(w) |
RTV2(r) |
| Aceton |
1 |
2 |
2 |
1 |
1 |
1 |
1 |
| Benzin |
3 |
3 |
3 |
2 |
2 |
3 |
3 |
| Salzsäure
2 mol/l |
2 |
1 |
1 |
1 |
1 |
1 |
1 |
| Salzsäure
10 mol/l |
2 |
2 |
1 |
3 |
1 |
2 |
3 |
| Natronlauge
2 mol/l |
1 |
2 |
2 |
1 |
1 |
1 |
1 |
| Natronlauge
50 % |
1 |
1 |
1 |
3 |
3 |
3 |
2 |
| Mineralöl |
3 |
1 |
1 |
1 |
1 |
1 |
1 |
| Schwefelsäure
1 mol/l |
1 |
1 |
1 |
1 |
1 |
1 |
1 |
|
 |
  Beim
Vergleich der Chemikalienbeständigkeit erkennt man, dass Silicone gegenüber
Mineralöl, Aceton, sowie relativ verdünnten Lösungen (c <
2 mol/l) anorganischer Säuren und Basen beständig sind. Dagegen
werden sie von konzentrierten Lösungen starker Säuren und Basen
und von Benzin angegriffen. Beim
Vergleich der Chemikalienbeständigkeit erkennt man, dass Silicone gegenüber
Mineralöl, Aceton, sowie relativ verdünnten Lösungen (c <
2 mol/l) anorganischer Säuren und Basen beständig sind. Dagegen
werden sie von konzentrierten Lösungen starker Säuren und Basen
und von Benzin angegriffen.
Die Abweichungen innerhalb der untersuchten Silicone können mit unterschiedlichen
Zusatzstoffen und Vernetzungsgraden erklärt werden.
Das beobachtete Verhalten der Silicone gegenüber Säuren und Basen
lässt sich mit der chemischen Struktur ihrer Moleküle erklären.
Aufgrund der Polarität der Siloxanbindung Si-O könnte das negativ
polarisierte Sauerstoffatom elektrophil angegriffen werden, wogegen das
positiv polarisierte Siliciumatom für nucleophile Angriffe zugänglich
ist.
Daraus sind die folgenden Reaktionen für den Abbau von Siliconen durch
anorganische Säuren und Basen theoretisch möglich (die gebogenen
Pfeile in den Formeln deuten jeweils die Verschiebung von Elektronenpaaren
an): |
 |
  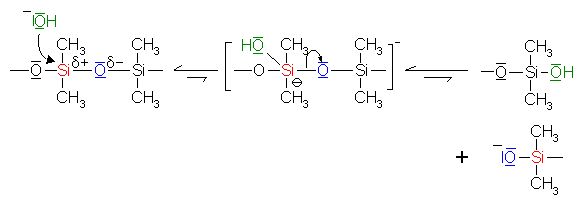 |
 Depolymerisation
von Siliconen durch Hydroxidionen Depolymerisation
von Siliconen durch Hydroxidionen |
 |
  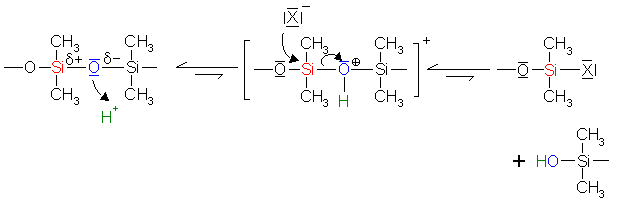 |
 Depolymerisation
von Siliconen durch anorganische Säuren HX Depolymerisation
von Siliconen durch anorganische Säuren HX |
 |
  Es
bedarf aber hoher Konzentrationen an Hydronium- bzw. Hydroxid-Ionen, also
konzentrierter Lösungen starker Säuren und Basen, damit diese
Reaktionen ablaufen. Dies erklärt, warum Silicone gegenüber verdünnten
Lösungen von anorganischen Säuren und Basen stabil sind. Es
bedarf aber hoher Konzentrationen an Hydronium- bzw. Hydroxid-Ionen, also
konzentrierter Lösungen starker Säuren und Basen, damit diese
Reaktionen ablaufen. Dies erklärt, warum Silicone gegenüber verdünnten
Lösungen von anorganischen Säuren und Basen stabil sind.
Bei der Einwirkung von Benzin auf Silicone handelt es sich nicht um eine
chemische Reaktion. Hier spielen vielmehr physikalische Vorgänge
eine Rolle. Das Aufquellen der Silicone in Benzin ist dadurch zu erklären,
dass unpolare Moleküle aus dem Benzin in das makromolekulare Siliconmaterial
eindringen und sich in das Molekülgeflecht einlagern.
Die untersuchten organischen Elastomere sind gegenüber sauren und
alkalischen Lösungen durchschnittlich bis sehr gut beständig.
Sie werden jedoch von organischen Substanzen wie Motoröl, Benzin
und Aceton angegriffen (Aufquellen, Lösen).
Die Beständigkeit der organischen Elastomere gegenüber Säuren
und Basen kann mithilfe ihrer Teilchenstruktur erklärt werden.
Allgemein sind organische Elastomere hauptsächlich aus ungesättigten
Polymeren aufgebaut. Naturkautschuk besteht aus cis-1,4-Polyisopren-Makromolekülen
(vgl. Abbildung), die beim Vulkanisieren über Schwefel-Atome miteinander
quervernetzt werden.
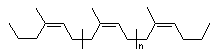 |
| Abb.: cis-1,4-Polyisopren (Naturkautschuk) Quelle:
Thieme Computerlexikon |
 |
  In den Polyisopren-Molekülen bieten sich als Angriffsstellen für
Reagenzien in erster Linie die Kohlenstoff-Kohlenstoff Doppelbindungen
an. Diese sind jedoch gegenüber direkten Angriffen von Nucleophilen
wie z.B. Hydroxid-Ionen stabil. Dagegen können Hydronium-Ionen aus
sauren Lösungen die Kohlenstoff-Kohlenstoff Doppelbindungen nach
dem Prinzip der elektrophilen Addition angreifen. So lässt sich erklären,
warum die untersuchten organischen Elastomere in konzentrierter Natronlauge
beständiger sind als in konzentrierter Salzsäure. In den Polyisopren-Molekülen bieten sich als Angriffsstellen für
Reagenzien in erster Linie die Kohlenstoff-Kohlenstoff Doppelbindungen
an. Diese sind jedoch gegenüber direkten Angriffen von Nucleophilen
wie z.B. Hydroxid-Ionen stabil. Dagegen können Hydronium-Ionen aus
sauren Lösungen die Kohlenstoff-Kohlenstoff Doppelbindungen nach
dem Prinzip der elektrophilen Addition angreifen. So lässt sich erklären,
warum die untersuchten organischen Elastomere in konzentrierter Natronlauge
beständiger sind als in konzentrierter Salzsäure.
Dass die untersuchten organischen Elastomere, die im wesentlichen aus
unpolaren Molekülen bestehen, in organischen Lösemitteln wie
Benzin, Aceton und Motoröl aufquellen und sich allmählich lösen,
liegt an den intermolekularen Wechselwirkungen zwischen den Molekülen
der Lösemittel und den Molekülen des organischen Elastomers
("Gleiches löst sich in Gleichem"). Es handelt sich dabei
vorwiegend um Van-der-Waals Kräfte. |
 |
  4
Tipps und Anmerkungen 4
Tipps und Anmerkungen
|
 |
- Als Alternative zu diesem Versuch wurde auch die
Chemikalienbeständigkeit der Elastomerproben bei Einwirkung von
Benzin, konz. Salzsäure, c = 10 mol/l, Natronlauge, w = 50 %, und
Aceton bei 45 °C untersucht. Die Elastomerproben wurden dabei zusammen
mit dem Medium in einen Rundkolben gegeben, verschlossen und dann mit
Hilfe eines Wasserbads eine Stunde lang auf ca. 45 °C erwärmt.
Dabei konnten bei konz. Salzsäure und Benzin dieselben Beobachtungen
gemacht werden wie im Langzeitversuch. Bei konz. Natronlauge und Aceton
konnten jedoch keine Veränderungen beobachtet werden. Die Ursachen
dafür liegen wohl in der zu geringen Reaktions- und Diffusionsgeschwindigkeit.
Daher reicht die Einwirkungszeit für eine sichtbare Veränderung
nicht aus.
- Als weitere Ergänzung zum Versuch wurden sämtliche
Proben vor und nach der Einwirkung der Medien mit Hilfe eines Mikroskops
bei 100 facher Vergrößerung untersucht. Es konnten jedoch
bei allen untersuchten Proben keine mikroskopischen Veränderungen
festgestellt werden. Aufgrund des hohen Zeitaufwandes sollte daher in
der Schule auf die mikroskopische Untersuchung der Proben verzichtet
werden.
- Durch den Versuch lernen die Schüler die chemische
Beständigkeit von Elastomeren und anderen Kunststoffen gegenüber
verschiedenen Medien zu ermitteln. Somit kann für jede praktische
Anwendung der optimale Kunststoff gewählt werden. Es wäre
z.B. wenig sinnvoll, Dichtungen aus Naturkautschuk in einer Benzinleitung
zu verwenden.
- In Bezug auf die Silicone wird den Schülern
dabei gleichzeitig das Verhalten von Siliconen gegenüber verschiedenen
Chemikalien, insbesondere anorganischen Säuren und Basen demonstriert.
Somit kommt auch hier wieder die didaktisch wichtige Relation zwischen
Stoffeigenschaft und Teilchenstruktur zum Tragen.
- Da der Versuch unter Beachtung der Sicherheitshinweise
(Handschuhe, Schutzbrille) relativ ungefährlich ist, eignet er
sich gut als Schülerversuch. Es empfiehlt sich aus zeitlichen und
kommunikativen Gründen, die Schüler in Gruppen arbeiten zu
lassen. Dabei untersucht jede Gruppe das Verhalten der Proben in einem
Medium. Die Proben sollten am Anfang oder Ende einer Stunde angesetzt
werden, um keine wertvolle Unterrichtszeit verstreichen zu lassen. Die
Auswertung kann dann in der nachfolgenden Woche erfolgen.
|
 |
  5
Ergänzende Sachinformationen 5
Ergänzende Sachinformationen
|
 |
Bei der Chemikalienbeständigkeit von
polymeren Materialien, wie z.B. Naturgummi (Naturkautschuk) oder Silicongummi
(Siliconkautschuk) kann die Chemikalieneinwirkung, je nach Art der Einwirkung
in zwei Gruppen eingeteilt werden.
- Physikalisch aktive Medien reagieren
nicht mit dem makromolekularen Material, tragen aber zur Quellung bis
zur Auflösung bei und bewirken dadurch reversible Veränderungen
der Eigenschaften des Materials.
Der Wirkungsmechanismus von physikalisch aktiven Medien beruht auf der
Zerstörung der intermolekularen Bindungen zwischen den Makromolekülen.
Beispiele für solche Medien sind chemisch inerte Kohlenwasserstoffe
und einige ihrer Derivate.
Aus Kunststoffen und Elastomeren, die Zusatzstoffen enthalten, können
die physikalisch aktiven Medien einige Zusatzstoffe (z.B. Weichmacher)
auslaugen, wodurch sich die Eigenschaften des Materials irreversibel
ändern.
Das Verhalten eines makromolekularen Materials gegenüber physikalisch
aktiven Medien kann annähernd mit der Polarität der beiden
Partner beurteilt werden. Allgemein gilt, dass Materialien aus unpolaren
Molekülen in unpolaren Lösungsmitteln quellen und aufgelöst
werden, während sie gegenüber polaren Verbindungen physikalisch
beständig sind. Makromoleküle mit polaren Gruppen sind in
polaren Lösungsmitteln löslich oder quellen, wogegen sie gegenüber
unpolaren Verbindungen beständig sind.
Die Beständigkeit von makromolekularen Materialien gegen physikalisch
aktive Medien ist noch von weiteren Faktoren abhängig, vor allem
von dem Vernetzungsgrad zwischen den Makromolekülen. Die Quellung
in Lösemitteln nimmt mit zunehmender Vernetzung ab. So quillt beispielsweise
Hartgummi in Kohlenwasserstoffen wesentlich weniger als Weichgummi.
Auch Füllstoffe können die Widerstandsfähigkeit von Polymeren
gegen physikalisch aktive Medien beeinflussen.
- Chemisch aktive Medien reagieren mit
dem makromolekularen Material und verändern seine Eigenschaften
irreversibel. Für den chemischen Abbau von Makromolekülen
ist charakteristisch, dass schon geringfügige chemische Veränderungen
sehr ausgeprägte Veränderungen der physikalischen Eigenschaften
hervorrufen können.
Dabei folgen makromolekulare Stoffe bei chemischen Reaktionen den gleichen
Gesetzmäßigkeiten wie niedermolekulare Stoffe. Der Reaktionsverlauf
ist jedoch bei makromolekularen und bei niedermolekularen Substanzen
verschieden.
Die Reaktion zwischen der aggresiven Chemikalie und dem makromolekularen
Material findet in der Regel in einem heterogenen System (fest / flüssig
oder fest / gasförmig) statt, weshalb ihr Verlauf ebenso wie die
Quellung und die Auflösung stark von Diffusionsvorgängen beeinflusst
wird. Die Folge ist, dass bei manchen chemischen Reaktionen zwischen
dem makromolekularen Material und dem einwirkenden Medium ein Film von
Reaktionsprodukten entsteht, der die Diffusion des Mediums hemmt und
somit die Abbaugeschwindigkeit des Materials verringert. Solche schützenden
Oberflächenschichten erklären die hohe chemische Beständigkeit
von Gummi aus Naturkautschuk gegenüber Salzsäure und Schwefelsäure.
Weiterhin wird die Beständigkeit von makromolekularen Materialien
gegen chemisch aktive Substanzen durch Füllstoffe oder sonstige
Zusatzstoffe in weiten Grenzen sowohl positiv als auch negativ beeinflusst.
Auch die Vernetzungsdichte hat einen Einfluss auf die chemische
Beständigkeit.
|
 |
  6
Literatur 6
Literatur |
 |
- M. Tausch, M. von Wachtendonk (Hrsg.), CHEMIE S II, STOFF-FORMEL-UMWELT,
C.C. Buchner, Bamberg (1993), (1998), S. 337 - 352
- M. Tausch, M. von Wachtendonk (Hrsg.), STOFF-CHEMIE S I, FORMEL-UMWELT,
C.C. Buchner, Bamberg (1996), (1997), S. 228 - 233
- M. Tausch, M. von Wachtendonk (Hrsg.), CHEMIE 2000+, C.C. Buchner,
Bamberg (2001), S. 60 - 67
|
 |
  | Home | Uni Wuppertal | WACKER | Didaktik | Sachinfo | Versuche | Medien | Kontakt | | Home | Uni Wuppertal | WACKER | Didaktik | Sachinfo | Versuche | Medien | Kontakt | |
|