|
8. Dissoziation des β-Cyclodextrin-Phenolphthalein-Komplexes |
||
Wenn man den Versuch zur Bildung des Wirt-Gast-Komplexes aus β-Cyclodextrin und Phenolphthalein durchgeführt hat, lässt sich dieser Versuch in zwei Minuten durchführen. |
||
|
||
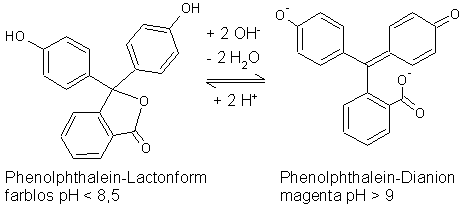
| Auch bei diesem Versuch nimmt man durch Veränderung der Hydroxidionen-Konzentration Einfluss auf das bestehende Gleichgewicht. Die veränderten Bedingungen zwingen einen Teil der komplexierten Phenolphthalein-Dianionen, den Wirt Cyclodextrin zu verlassen. Eine weitere Erklärung für die Verfärbung der Lösung findet man bei Betrachtung des Gleichgewichts zwischen dem Phenolphthalein-Dianion und der Phenolphthalein-Lactonform. | ||
 |
||
| Abb. 2.18: Molekülstrukturen von Phenolphthalein bei pH < 8,5 und pH > 9 | ||
| Wenn das Gleichgewicht bei pH > 9 nicht vollständig auf der Seite des Dianions liegt, dann führt eine Zugabe der Hydroxidionen zu einer Verschiebung des Gleichgewichtes auf die rechte Seite. Sind alle Cyclodextrin-Moleküle bereits mit Gast-Molekülen besetzt, dann liegt die Dianion-Form in der Lösung vor und führt zu der beobachteten rotvioletten Farbe der Lösung. | ||