|
8. Wirt-Gast-Komplex mit thermochromen und photochromen Eigenschaften |
||||||||||
Die Herstellung des Komplexes benötigt sechs Stunden Rührzeit. Nachdem der Feststoff abgenutscht und getrocknet wurde, kann er ihm Unterricht eingesetzt werden. Die Untersuchung der thermochromen und photochromen Eigenschaften ist innerhalb von 15 Minuten durchführbar. Die Chemikalie Spiropyran kann im Chemikalienhandel bestellt oder in einer einstufigen Synthese hergestellt werden. |
||||||||||
|
||||||||||
In diesem Versuch wird ein Wirt-Gast-Komplex mit dem größten der drei natürlichen Cyclodextrine und Spiropyran (siehe Abb. 2.38) gebildet. Spiropyran liegt zunächst als neutrales Molekül vor und ist aufgrund seiner Molekülstruktur nicht wasserlöslich, so dass eine Komplexbildung aus einer wässrigen Lösung nicht möglich ist. Deshalb wird als Lösemittel Ethanol mit einem kleinen Wasseranteil verwendet. In der Suspension bildet sich während des Rührens ein Komplex, in dem zwei γ-Cyclodextrin-Moleküle ein Spiropyran-Molekül umschließen (siehe Abb. 2.37). |
||||||||||
 |
||||||||||
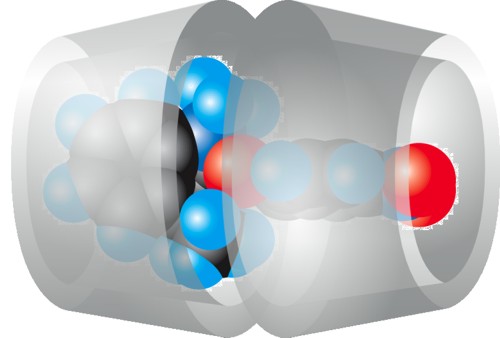
| Abb. 2.37: Der γ-Cyclodextrin-Komplex mit Spiropyran hat die Stöchiometrie Wirt : Gast = 2 : 1 | ||||||||||
| In diesem Cyclodextrin-Komplex werden jeweils Teile des Spiropyran-Moleküls über van-der-Waals-Kräfte in den Cyclodextrin-Hohlräumen stabilisiert. Der rechte Molekülteil (siehe Abb. 2.38) kann mit der Nitrogruppe auch eine Wasserstoffbrückenbindung zu den primären Hydroxygruppen am unteren Rand des Cyclodextrin-Moleküls eingehen. | ||||||||||
 |
||||||||||
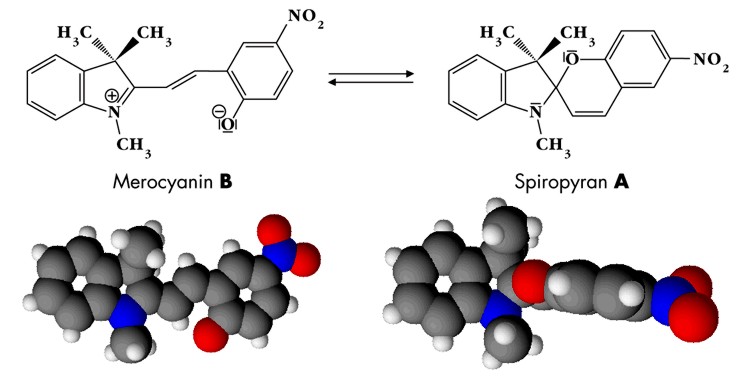
| Abb. 2.38: Molekülstrukturen und Kalottenmodelle der Isomere Merocyanin und Spiropyran | ||||||||||
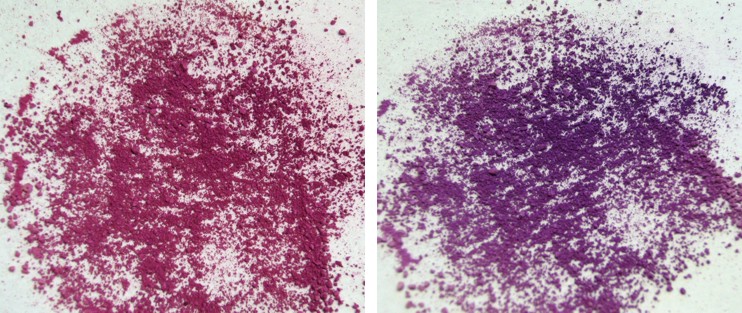
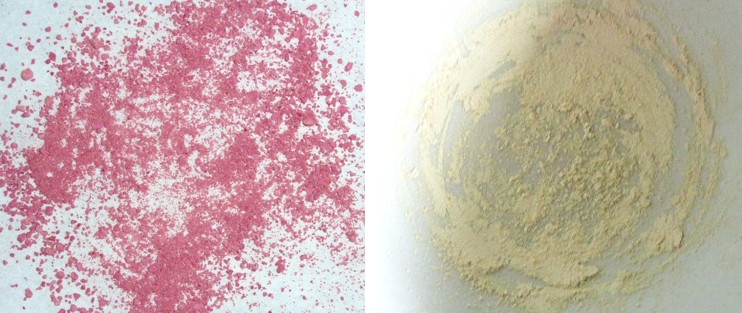
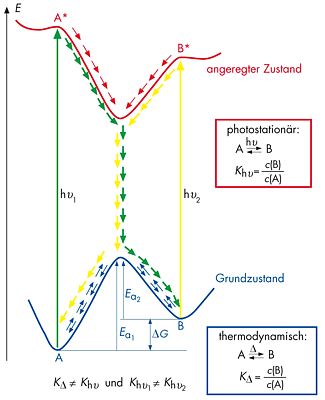
| Die beobachteten Farbänderungen bei Licht- oder Wärmeeinwirkung zeigen, dass es trotz der Komplexierung in den Cyclodextrin-Molekülen zur Isomerisierung kommen kann. Die zwischenmolekularen Wechselwirkungen zwischen den Cyclodextrin-Molekülen und Teilen des Gast-Moleküls werden bei der Isomerisierung aufgehoben und müssen sich dann wieder neu ausbilden, denn die räumlichen Strukturen des Merocyanins und Spiropyrans unterscheiden sich stark. Durch Bildung des Spiropyrans aus dem Merocyanin bildet sich ein Spirozentrum aus, an dem sich die beiden Molekülteile senkrecht zueinander anordnen und starr sind (siehe Kalottenmodell in Abb. 2.38), während das Merocyanin-Molekül um die Einfachbindungen im mittleren Teil drehbar sind. Das System konjugierter Doppelbindungen ist im Merocyanin wesentlich größer als im Spiropyran, so dass man die blauviolette Farbe des Feststoffes auf die Bildung von Merocyanin zurückführen kann. Bestrahlt man den Feststoff mit sichtbarem Licht, dann bildet sich das Spiropyran, in dem aufgrund des Spirozentrums kein ausgedehntes System konjugierter Doppelbindungen vorliegt. Die Farbe rosa ist dann zu beobachten, wenn die beiden Isomere im Gleichgewicht vorliegen. Abb. 2.39 zeigt das Energiediagramm, in dem die Energieniveaus der beiden Isomere A und B im Grundzustand und in den elektronisch angeregten Zuständen A* und B* dargestellt sind. Das thermodynamisch stabilere Isomer A ist das Spiropyran, das im Versuch durch thermische Isomerisierung zu dem violett gefärbten Merocyanin (B) reagiert. Mit dem Schema lässt sich erklären, warum die Rückfärbung zu dem rosa gefärbten Feststoff schnell erfolgt. Durch Wärmezufuhr ist genügend Aktivierungsenergie vorhanden, um wieder in den thermodynamisch stabileren Zustand A zu gelangen (blaue Kurve in Abb. 2.39). Doch diese Rückreaktion B → A verläuft nicht vollständig, so dass Spiropyran und Merocyanin in einem Gemisch vorliegen. | ||||||||||
 |
||||||||||
| Abb. 2.39: Energiediagramm zum System Spiropyran – Merocyanin | ||||||||||
| Bei der Einstrahlung von Licht findet eine photochemische Isomerisierung statt, bei der das Merocyanin durch Absorption eines geeigneten Lichtquants in den angeregten Zustand übergeht, um dann zu Spiropyran (A) zu reagieren (in Abb. 2.39 gelb dargestellt). Da Spiropyran thermodynamisch stabiler ist, erfolgt hier keine Rückreaktion, so dass die gelbliche Farbe lange erhalten bleibt. Das Gleichgewicht zwischen den Isomeren liegt dann stark auf der Seite des Spiropyrans (A). | ||||||||||
| Die Komplexierung von Spiropyran ist mit β-Cyclodextrin nicht möglich. Der Feststoff ist nicht gefärbt. Das β-Cyclodextrin-Molekül hat einen zu geringen Innendurchmesser für das Spiropyran. Das komplexierte Spiropyran kann als molekularer Schalter fungieren, der entweder durch Licht oder Wärme in die eine oder andere Form geschaltet werden kann. Die Photochromie und die Thermochromie des Spiropyran-Merocyanins können auch beobachtet werden, wenn Spiropyran in Toluol oder in Nagellack gelöst wird. | ||||||||||
Im Versuch wurde die Isomerisierung von Spiropyran zum Merocyanin nur auf thermischem Weg erreicht. Man kann die Bildung des Merocyanins auch auf photochemischem Wege erreichen. Dazu ist wegen der größeren Energiedifferenz zwischen dem Grundzustand und dem angeregten Zustand des Spiropyrans energiereicheres Licht nötig. Um Spiropyran anzuregen, benötigt man UV-Licht, das von einem wassergekühlten 150W-Quecksilberhochdruckbrenner ausgestrahlt wird. Im Licht dieser Lampe kann man nach einiger Zeit eine Violettfärbung des Feststoffs beobachten. Um auszuschließen, dass die Isomerisierung nicht thermisch erfolgt, wird die Quecksilberhochdrucklampe mit Wasser gekühlt und die Temperatur mit einem Thermofühler kontrolliert. |
||||||||||
 |
||||||||||
| Abb. 2.40: Die photochemische Isomerisierung von Spiropyran nach Merocyanin gelingt nur mit energiereichem UV-Licht | ||||||||||
|
||||||||||